
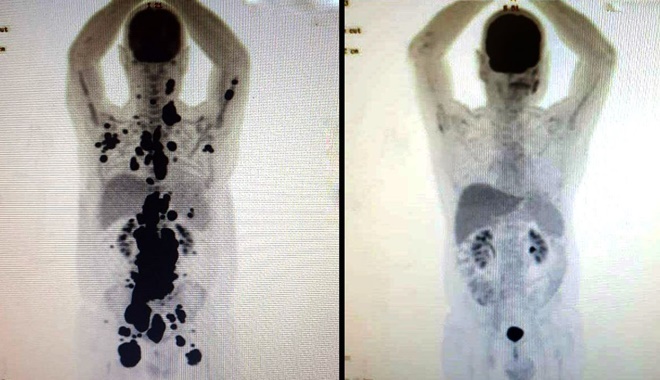
Terapia celular CAR-T Cell
Anvisa aprova estudo clínico de tratamento para leucemia e linfoma usando células CAR-T em pacientes brasileiros. Estudo é desenvolvido por pesquisadores brasileiros; calendário prevê ações até dezembro de 2024
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou um ensaio clínico no Brasil com medicamento a base de células geneticamente modificadas, ou células CAR-T, que pode ser um avanço no tratamento contra o câncer no sangue.
O estudo clínico de fase 1/2 vai incluir 81 pacientes com leucemia linfoide aguda de células B e linfoma não Hodgkin de células B, com o produto de células CAR-T, deve ser realizada pela Fundação Hemocentro de Ribeirão Preto (FUNDHERP), em parceria com o Instituto Butantan e USP, com o apoio de instituições de fomento como a Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) e o Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq). A aprovação foi divulgada no último dia 26, pela autarquia responsável pela defesa da saúde dos brasileiros.
A iniciativa será realizada gratuitamente em cinco hospitais do Estado de São Paulo, dentre eles o Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto (HCFMRP) da USP e o Hospital das Clínicas (HC) da Faculdade de Medicina da USP (FMUSP). Foram construídas duas unidades do Núcleo de Terapia Avançada (Nutera), em Ribeirão Preto e São Paulo.
O tratamento consiste em reprogramar as próprias células do paciente para atacar e destruir o câncer, em casos de reaparecimento da doença ou de resistência ao tratamento convencional.
As pesquisas estão em fase clínica inicial e sua segurança e eficácia serão avaliados, informou a Anvisa.
De acordo com a agência, a aprovação “envolve revisões frequentes dos dados e informações da pesquisa, com ações planejadas até dezembro de 2024, para monitorar de perto o desenvolvimento do produto”.
“Se os resultados forem bons, o objetivo é registrar o produto rapidamente para que as pessoas tenham acesso a uma opção de tratamento segura, eficaz e de alta qualidade disponível no SUS“, afirmou a agência.
Segundo informações do Instituto Butantan, o primeiro voluntário brasileiro a receber um tratamento experimental com células CAR-T, em 2019, apresentou remissão total de um linfoma em estágio terminal.
Saiba mais: Paciente com câncer terminal tem remissão total após terapia celular em estudo na rede pública
Esse tipo de terapia, criada nos Estados Unidos, vem sendo testada desde 2010. Nos Estados Unidos, os resultados positivos levaram à aprovação do tratamento pela agência reguladora americana Food and Drug Administration (FDA), em 2017.
Orientações de como participar do estudo clínico e informações sobre a terapia com células CAR-T estão no site: hemocentro.fmrp.usp.br/terapia.
→ SE VOCÊ CHEGOU ATÉ AQUI… Saiba que o Pragmatismo não tem investidores e não está entre os veículos que recebem publicidade estatal do governo. Fazer jornalismo custa caro. Com apenas R$ 1 REAL você nos ajuda a pagar nossos profissionais e a estrutura. Seu apoio é muito importante e fortalece a mídia independente. Doe através da chave-pix: pragmatismopolitico@gmail.com

